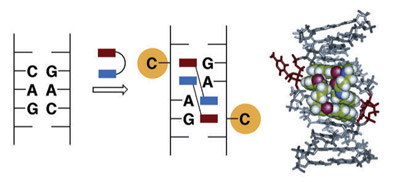
| 図1:アルツハイマー病のin vivoイメージング | |
 |
|
見えないものを見る
アミロイドB沈着に対する新たな化学プローブが、in
vivoでのアルツハイマー病(AD)の検出にどのように役立つのかを、2件の報告が明らかにしている。
ある疾患の決め手となるものが脳の中に埋もれているとすれば、その疾患を検出するにはどうすればよいのであろうか? それが長年AD研究者を悩ませてきた問題である。ADの原因はいまだに不明であるが、機能的障害の発現より10〜20年先行して、アミロイドBペプチドから成るプラークの形成が生じていることが知られている。したがって、早期検出はADの研究や診断にとって朗報であろう。残念ながら、頭蓋骨や血液脳関門という外側に対する防御のために、内側の障害が容易に検出できないという逆説的な事態が生じている。
コンピュータ断層撮影(CT)や磁気共鳴画像(MRI)などの脳画像診断法は、脳内の物理的構造を描出するのには適しているが、ADの症状に先行する小さなプラークを検出するには不十分である。血液脳関門透過性の化合物を注射することによって、画像コントラストは改善する可能性がある。陽電子放射断層撮影(PET)は、小さな機能的・病理学的変化の検出により適しているが、短命で危険をもたらす可能性のある放射性マーカーの注射が必要となる。
研究者らはADの初期の決め手となるものを検出しようと試みているが、成功の度合いはさまざまである。群を抜いて大きな成功を収めている手法は、脳機能の初期変化と併せてアミロイド沈着を描出する能力をもつPETであり、現在、病院で初期ADの診断に使用されている。残念なことにPETは、ADマウスモデルにおけるアミロイドプラークの描出には成功していない。このような不都合に加え、高コストと複雑さを伴うため、PETはほとんど研究目的には適さないものとなっている。
ノバルティスファーマ社のin
vivo画像部門(in vivo imaging group at Novartis)に所属するHans-Ulrich
Gremlichは、創薬の研究においてADマウスモデルに使用できるイメージングツールを探していた。Gremlichは、近赤外蛍光(NIRF)イメージングは簡便で低コストであることから、ハイスループットスクリーニングのための優れた選択となると考えた。しかし、それを実現するには、in
vivoでアミロイドプラークを標的とする能力をもつNIRFリガンドが必要であった。「この研究のために学位取得者を雇う許可が得られたのは運が良かった。Martin
Hintersteinerはこの研究にうってつけの人物で、朝早くから夜遅くまで働いてくれました」とGremlichは述べている。この熱意の結果が、NIRFリガンドである。このリガンドは、ADモデルマウスにおいて、血液脳関門を透過し、特異的にアミロイドプラークと結合して、プラークレベルに関する定量的情報を提供することができる(Hintersteiner
et al.,
2005、図1a)。Gremlichは、この発見が示している進歩について次のように説明している。「以前は、毎回の測定後に動物を殺して組織学的検査を行わなければなりませんでしたが、いまでは、同じ動物を使って縦断的研究を行うことができます。これは、いま私たちに与えられた絶好の機会であり、まったく新しいチャンスなのです。」
NIRFリガンドの開発が進められているあいだに、日本のあるグループが、別の蛍光化合物によるアミロイドプラークの染色について試験していた(Sato
et al.,
2004)。その蛍光物質は可視スペクトル内にあるため、顕微鏡法でしか使用されていなかったが、開発者らは、MRIで使用できる可能性があることに気付いた。好都合なことに、この化合物にはフッ素が含まれていた。著者の樋口真人(Makoto
Higuchi)は「体内には、バックグラウンドノイズの原因となる可能性のある内因性のフッ素が存在しないので、フッ素MRI技術によって、高コントラストのin
vivo画像を得ることができるのではないかと予測したのです」と述べている。樋口らは、自ら合成した化合物をMRIに用いることによって、ADマウスモデルで個々のプラークを検出することができ、また、プラークが最初に出現する小さな解剖学的構造でも検出が可能であることを立証している(Higuchi
et al.,
2005、図1b)。現在のMRI技術ではこの手法によって得られるシグナルが弱いため、「[この手法は]ヒト被験者のイメージングにすぐに応用できるというわけではありません。フッ素MRIを用いたヒト脳内のアミロイドプラークの描出は、検出システムの感度を改善することによって可能となるでしょう」と樋口は述べている。
マウスにおいてプラークが発生する過程を追って繰り返し撮像することを可能にするこのような技術は、刺激的で新たな可能性を開いてくれる。現在では、疾患の進行との相関を示す、容易に測定できる生物学的マーカーを探索することが可能となっている。このことは、とくにNIRFイメージングの場合に当てはまる。なぜなら、樋口氏が言うように、「低用量の光学的トレーサ(optical
tracer)を用いることによって、毒性を引き起こすことなく、同じ動物で反復測定を行えるようになる」からである。これは最終的に、病院でADを診断するさいにイメージングがほとんど必要なくなるという例をみない事態をもたらすことになるであろう。
Daniel
Evanko
|
||||||
関連情報
脳内のβアミロイド分解経路を解明
誕生近し!アルツハイマー薬(All About)
認知症・アルツハイマー
アリセプト(塩酸ドネペジル)
血液脳関門
ミクログリアを用いたバイオターゲティング
| SEO | [PR] 爆速!無料ブログ 無料ホームページ開設 無料ライブ放送 | ||
